 当前位置: AI资讯 > 内文
当前位置: AI资讯 > 内文2022-6-24 关键词:临床科研
6月23日,经国家药品监督管理局审核同意,国家药监局药审中心发布《药物临床试验期间方案变更技术指导原则(试行)》(以下简称《指导原则》),文件自发布之日开始施行,旨在指导药物临床试验申办者规范开展临床试验期间方案变更相关工作。

本《指导原则》适用于与注册相关的中药、化药、生物制品(含疫苗)相关的临床试验方案变更。不适用于临床试验期间改变剂型、给药途径、新增适应症以及增加与其他药物联合用药等情形,上述情形不属于方案变更管理范 畴,应按相关要求提出新的临床试验申请。
药物临床试验期间方案变更是指药物临床试验期间,因各种原因,需要对药品审评机构已批准或经沟通交流认可的临床试验方案内容进行修改或完善。主要包括以下几方面:
1.临床试验期间,发现药物新的安全性问题或潜在安全风险;
2.临床试验期间,需要对临床试验有效性研究相关内容进行修改或完善;
3.临床试验期间,为了提高临床试验实施效率,需要修改试验方案中相关内容;
4.其他,如变更联系人、联系方式等,一般不涉及试验方案设计的变化。
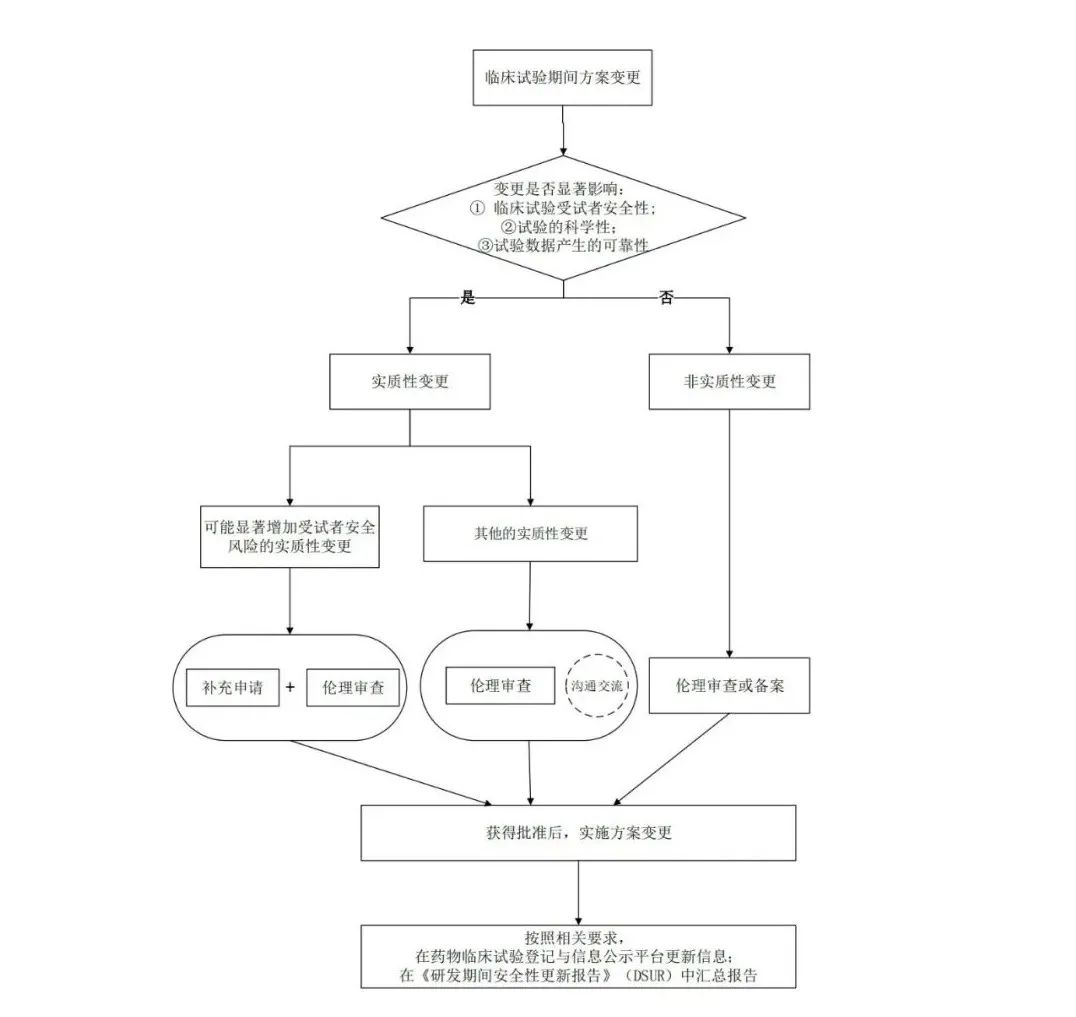
临床试验期间方案变更示意图
药物临床试验期间,在方案变更前,还应全面、深入评估方案变更的必要性和科学合理性。应结合非临床安全性和有效性研究、药学工艺、质量标准、稳定性研究等,以及临床试验的不同阶段和性质,如首次人体试验、探索性试验、确证性试验等,对方案变更后临床试验的整体设计、实施、预期有效性结果、统计分析、风险控制、风险-获益权衡等重新进行评估,判断是否可能产生显著性影响。
成为我们的
合作伙伴
